
近日,广州医科大学附属第一医院杨海虹教授团队联合天津市临床多组学重点实验室在 International Journal of Medical Sciences 上发表了一篇题为“Proteomics-based Model for Predicting the Risk of Brain Metastasis in Patients with Resected Lung Adenocarcinoma carrying the EGFR Mutation”的文章,基于液相色谱-质谱联用(LC-MS/MS)技术构建了一种蛋白质标志物预测模型来精确预测携带 EGFR 突变的肺腺癌患者术后脑转移风险,对于临床初次手术后患者的个体化精准治疗具有重要意义。
脑转移(BMs)是 EGFR 突变肺腺癌患者的常见并发症,发生率高且与不良预后密切相关。辨别脑转移高危人群并进行有效干预对于减少或延缓 BM 的发生具有重要意义。目前尚缺乏有效的工具评估,鉴于 BM 的高发病率,迫切需要开发新的生物标志物。
|研究方法|
对 2012 至 2018 年间广州医科大学第一附属医院招募的 56 名受试者进行回顾性分析,所有患者均为携带 EGFR 突变、经根治性切除后复发的肺腺癌(LUAD)患者。将患者分为脑转移组(BM,n=28)和非脑转移组(NBM,n=28),利用 LC-MS/MS 技术进行组织蛋白质组学检测。为了识别预测 LUAD 脑转移的潜在标志物,对不同组别进行比较分析,以评估与脑转移相关的蛋白质。
|研究结果|
研究显示,复发患者的临床因素与脑转移发生之间没有显著相关性。在蛋白组学层面,识别脑转移组和非脑转移组间的差异蛋白,筛选出区分两组性能最优的的 8 种蛋白(RRS1、CPT1A、DNM1、SRCAP、MLYCD、PCID2、IMPAD1和FILIP1)。基于随机森林算法利用这八种蛋白构建出最佳模型,其 ROC 值达到 0.9401,表明该模型在区分 BM 组和 NBM 组方面表现优异。
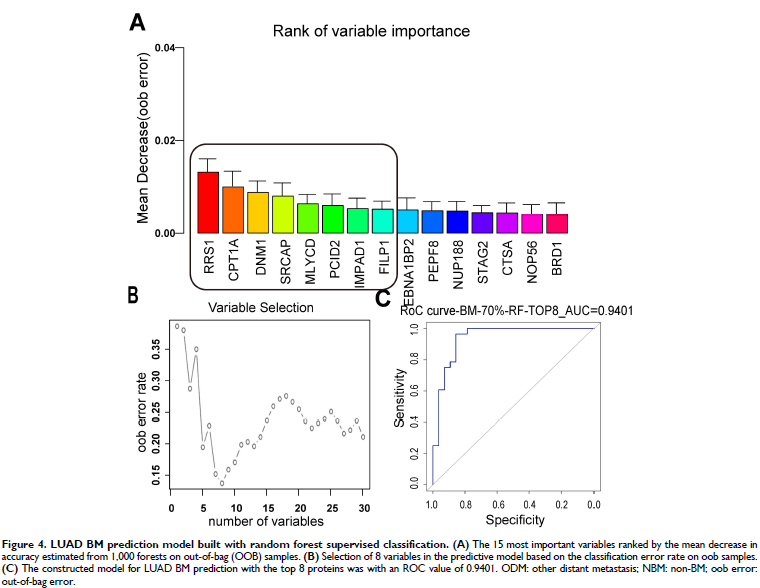
进一步分析脑转移发生的潜在机制,对两组差异蛋白进行 GO 富集分析,结果显示 BM 组主要表现为参与脂质代谢的蛋白上调,而细胞周期通路相关蛋白表达下调。亚组分析显示术后接受不同辅助治疗方案的患者其蛋白特征差异显著。接受化疗的脑转移患者,主要表现为参与染色体组装、核相关通路蛋白显著下调,参与脂质代谢和免疫相关通路蛋白上调。而接受 TKI 治疗的脑转移患者上调蛋白主要富集在与细胞黏附、膜组织、炎症反应等膜改变相关通路,下调蛋白富集在与代谢物相关的通路上。
|研究结论|
本研究基于蛋白生物标志物开发了一个可精准预测 EGFR 突变肺腺癌患者术后脑转移风险的模型,对于患者术后管理具有重要的参考价值。
目前 LC-MS/MS 临床检验方法绝大多数是实验室自建方法,因实验室使用的仪器、试剂、标准品等不同,需设置不同的检测参数,导致自建的检测方法存在很大差异,给 LC-MS/MS 检测的标准化带来很大困难。
谱天生物多款样本前处理试剂盒的获批,解决了 LC-MS/MS 临床检验过程无标准、无质控的弊端,极大程度改善不同实验室在使用质谱检测组织蛋白过程中遇到的以上障碍和可比性问题,有助于进一步改进 LC-MS/MS 方法在临床上的应用现状,加快实现蛋白质组学的临床转化。

代表产品
PT-L1TM Ⅰ 期肺癌患者术后复发风险预测
ProteinT-Lung1TM (PT-L1TM)采用 LC-MS/MS 技术对患者肿瘤组织进行蛋白质组学检测,基于模型计算患者复发风险评分,评估患者术后 5 年复发风险。 PT-L1TM 的灵敏度和特异性高达 96% 和 86%,阴性预测值(NPV)高达 98%,可精准地评估复发风险,为患者带来明确的临床获益。