
糖尿病是动脉粥样硬化性心血管疾病(ASCVD)的重要独立危险因素,ASCVD是糖尿病患者常见并发症和重要死亡原因。在糖尿病患者中血脂异常的发病率和心血管疾病导致的死亡率显著高于非糖尿病患者,但目前血脂异常的知晓率、治疗率和达标率均不容乐观。为了更好的规范我国糖尿病患者的血脂管理,中国医师协会内分泌代谢科医师分会和国家心血管病专家委员会心血管代谢医学专业委员会组织专家,根据中国糖尿病患者的血脂管理现状,参考国内外新的循证证据和指南,制定了《糖尿病患者血脂管理中国专家共识(2024版)》。

谱天生物核磁共振波谱技术(NMR),解决了当前传统血脂指标不够精准的痛点。是检测低密度脂蛋白颗粒(LDL-P)及亚组分不可替代的工具,对心血管疾病(ASCVD)的预警和治疗作用已被大量文献报道,LDL-P同时也是国际权威糖尿病指南血脂控制的重要指标。稳定性及准确性极佳,被国内外相关权威指南共识推荐。
指南解读
1 糖尿病患者的血脂谱特点及心血管危害
2型糖尿病(T2DM)或血糖控制不佳的1型糖尿病(T1DM)患者的血脂谱主要表现为混合型血脂紊乱,包括空腹或餐后高甘油三酯血症,伴HDL-C水平降低及小而密的低密度脂蛋白(sdLDL)水平增加。对于血糖控制良好的T1DM患者其sdLDL仍高于正常人群。在糖尿病患者血脂异常所带来的心血管风险中,LDL-C是公认的首要危险因素,而sdLDL因在血液中循环时间长、更易进入动脉血管内膜下并滞留,较LDL具有更强的致动脉粥样硬化作用。非HDL-C代表了全部致动脉粥样硬化脂蛋白颗粒中的胆固醇,该指标异常升高可作为预测ASCVD风险的重要因素。
2 糖尿病患者的ASCVD危险分层与治疗目标
根据患者病程长短、是否合并ASCVD及主要靶器官损害情况,将糖尿病患者分为超高危、极高危和高危(表1),以便于开展ASCVD风险评估,并基于风险分层制定血脂干预靶点及目标值推荐(表2)。LDL-C、非HDL-C作为首要降脂靶点,ApoB作为ASCVD风险干预的次要靶点。TG、Lp(a)及HDL-C异常均与ASCVD风险增加有关,但是目前缺乏较强证据支持药物干预这些血脂指标能降低ASCVD风险,因此将其列为糖尿病患者ASCVD风险管控的潜在调脂靶点,临床也需予以关注。

3 糖尿病患者的降脂治疗策略
糖尿病患者的降脂达标策略包括生活方式干预和药物治疗(表3)。

01
生活方式干预
无论合并哪种类型的血脂异常,健康均衡的膳食均需贯穿生活方式干预始终。膳食方面要限制总脂肪、饱和脂肪酸、胆固醇和反式脂肪酸的摄入,适量增加不饱和脂肪酸(植物油),特别是富含ω‑3多不饱和脂肪酸的食物。增加蔬菜水果、粗纤维食物的摄入,高TG血症患者还需减少精致碳水,增加纤维含量丰富的低糖饮食(如全谷类的粗粮)。运动方面每周应进行150min以上的中等强度运动,减重者还需继续增加每周运动强度和时间。如血糖波动大、有其他靶器官损伤等情况下不宜运动者,需待病情稳定后方可逐步恢复运动。通过控制总热量摄入及增加运动量,将体重指数维持在24 kg/m2以内。升高HDL-C还需戒烟(包括电子烟),降低TG则需不饮酒或限量饮酒(酒精摄入量男性<25 g/d,女性<15 g/d),高TG血症者更需严格限制酒精摄入。
02
降胆固醇药物治疗策略
生活方式干预难以降脂达标者,建议在生活方式干预的同时启动药物治疗,加快降脂达标减少ASCVD事件。糖尿病患者的降胆固醇治疗策略和流程见图1。
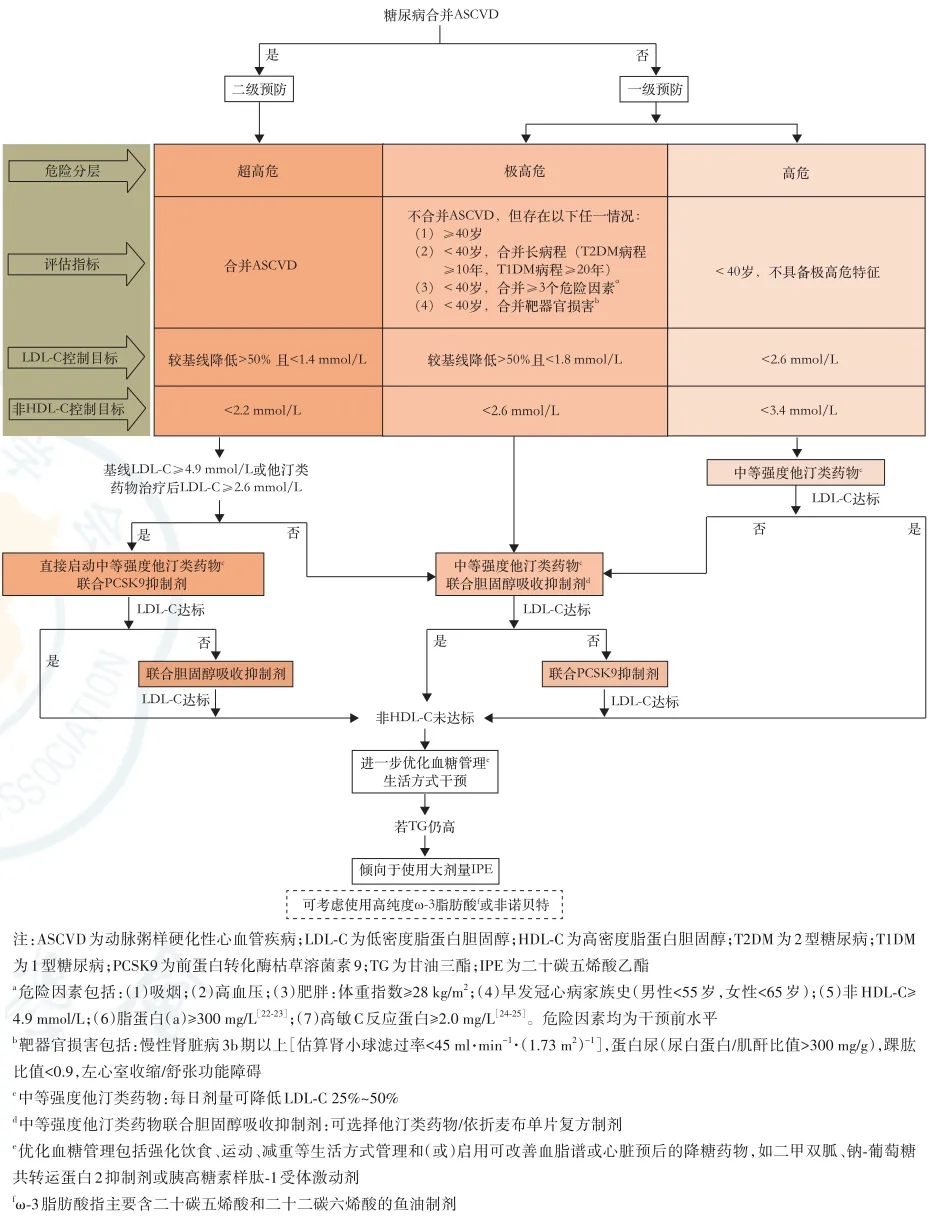
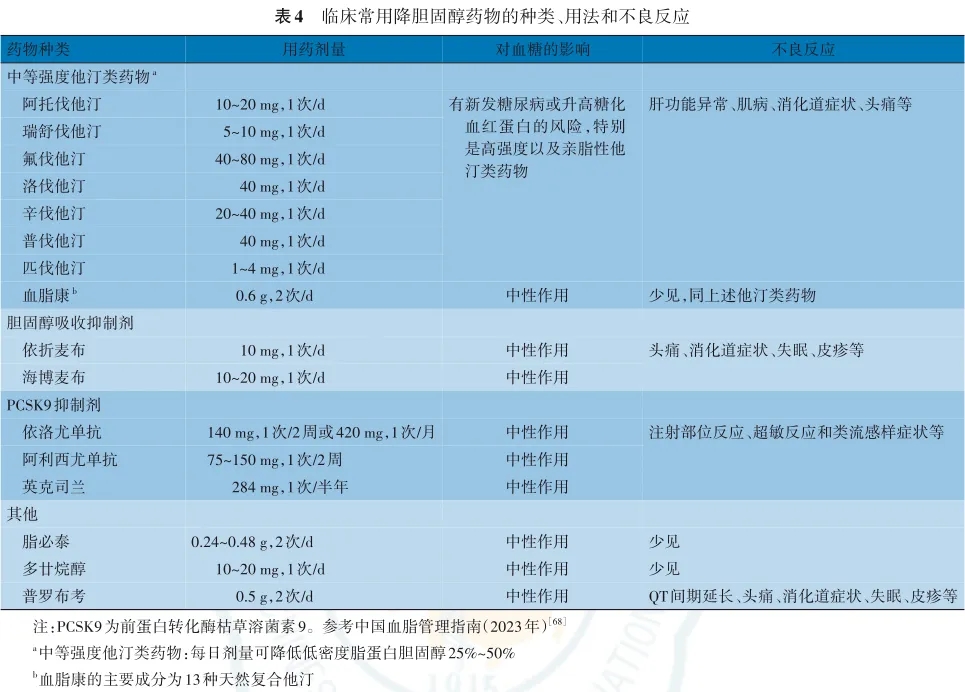
降胆固醇药物根据机制可分为三大类,包括他汀类药物、胆固醇吸收抑制剂和PCSK9抑制剂(表4)。他汀类药物作为降胆固醇治疗的基础药物,可促进肝细胞摄取并清除血液中的LDL颗粒,显著降低血清TC、LDL-C和ApoB水平。多项研究结果证实,他汀类药物可显著减少糖尿病患者的ASCVD事件。我国人群对大剂量他汀类耐受性差,因此不建议使用高强度他汀类药物,推荐使用中等强度作为初始降脂方案。胆固醇吸收抑制剂包括依折麦布、海博麦布,可抑制肠道对膳食和胆汁胆固醇的吸收。依折麦布联合他汀类药物为合并糖尿病的急性冠状动脉综合征患者带来更大获益,其中心肌梗死、缺血性脑卒中和主要终点事件发生风险显著下降。PCSK9抑制剂可增加血清LDL的清除而降低LDL-C水平,还可改善TG、ApoB和Lp(a)。PCSK9单克隆抗体助力大多数ASCVD高危/极高危的T2DM患者血脂快速达标,安全性、耐受性良好,且不影响血糖水平。此外,临床上尚有其他降胆固醇药物,如血脂康、胆汁酸螯合剂、普罗布考、脂必泰、多廿烷醇等。
03
降TG治疗策略
糖尿病患者的TG管理策略见表5。

04
降低Lp(a)治疗策略
目前尚无针对Lp(a)治疗的药物应用于临床,对于Lp的控制主要以降低胆固醇为主,PCSK9抑制剂可将糖尿病患者的Lp(a)水平降低约20%-30%,且显著减少MACE发生,可作为临床用药选择。
05
降脂药物对血糖的影响及处理策略
降脂药物影响血糖的机制尚未完全清楚。研究显示他汀类药物和烟酸类药物对血糖控制不利并有增加新发糖尿病的风险,但鉴于他汀类药物对心血管的保护作用远大于其不利效应,且不同种类、不同剂量对血糖的影响不同,故不推荐糖尿病患者因血糖控制不良而停服。可在血脂控制达标的基础上,尽量选择对血糖影响较为中性及临床效价比高的中等强度他汀类药物,并在使用前和使用中加强血糖或HbA1c监测。若血脂控制不达标,可考虑联用其他药物,而不建议增加他汀类药物剂量。胆固醇吸收抑制剂、PCSK9抑制剂、普罗布考、贝派地酸、贝特类药物、高纯度ω‑3脂肪酸对血糖调节呈中性作用,部分研究结果还显示上述药物可在一定程度上改善糖代谢、减轻胰岛素抵抗以及脂肪肝。胆汁酸螯合剂虽可同时改善糖脂代谢,但降脂效果较弱,消化道不良反应较大,我国临床应用甚少。对于降低Lp(a)的新药目前临床研究仍在进行中,其长期应用对血糖的影响尚不明确。
06
降脂治疗过程中的监测
对于首次服用降脂药物者,应在用药4~6周时复查血脂、肝酶、肌酸激酶等指标。如血脂达标,且无药物不良反应,逐步改为每3~6个月复查一次。如治疗4~6周后,血脂仍未达标,需及时调整降脂药物剂量或种类,或联合应用不同作用机制的降脂药物。每当调整降脂药物种类或剂量时,都应在治疗4~6周时复查。此外,鉴于长期服用他汀类药物可能引起糖代谢异常,应同时加强对血糖和(或)HbA1c 的监测。
4 糖尿病特殊人群的降脂治疗
01
儿童与青少年
建议对诊断为糖尿病的10岁以上儿童和青少年在血糖得到控制后或接受降糖药物治疗3个月后进行血脂检测和评估。儿童与青少年糖尿病患者理想的血脂水平为 LDL‑C<2.6 mmol/L,HDL‑C>0.9 mmol/L,TG<1.7 mmol/L,非HDL‑C<3.4 mmol/L。对于持续血脂异常者应进行干预将血脂控制在理想范围内。干预措施以低脂与高纤维饮食、规律运动、保持理想体重及保持充足睡眠等健康生活方式及优化血糖控制为基础。合并家族性高胆固醇血症者可考虑启动降脂治疗,降脂药物包括他汀类药物、依折麦布、胆汁酸螯合剂和PCSK9抑制剂,但这些药物在儿童和青少年中使用的长期安全性证据有限。
02
≥75岁老年人
≥75岁的糖尿病患者均为ASCVD极高危患者,建议积极进行降脂治疗。研究证实这类患者亦能从降低LDL-C的治疗中获益,但共识对LDL‑C目标值不做明确推荐。对于高龄老年患者,可考虑中等强度他汀类药物联合非他汀类药物(依折麦布、PCSK9抑制剂等)作为强化降脂治疗的手段。用药过程中应加强对肝肾功能、肌肉受损等不良反应的监测。
03
合并慢性肾脏病(CKD)的患者
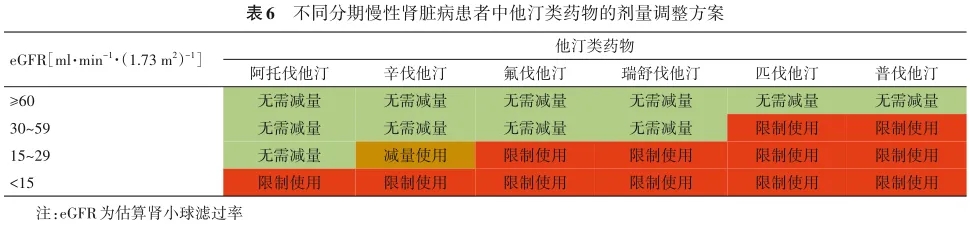
合并CKD的糖尿病患者心血管死亡风险显著增加,直接归入ASCVD极高危人群。对于轻中度肾功能不全的非透析患者,他汀类药物治疗可显著降低全因死亡风险,联用胆固醇吸收抑制剂或PCSK9抑制剂亦可带来心血管获益。但他汀类药物未能显著降低血液透析患者的心血管疾病发生风险。CKD患者应避免大剂量使用他汀类药物,不同CKD分期时他汀类药物的剂量调整方案见表6。胆固醇吸收抑制剂和PCSK9抑制剂对于肾功能受损患者是安全的,不需要调整剂量。
04
合并代谢相关脂肪性肝病(MAFLD)的患者
MAFLD指基于病理学或影像学存在脂肪肝证据,同时有超重/肥胖、T2DM或代谢功能紊乱3项条件之一者,是ASCVD的独立危险因素,糖尿病合并MAFLD者具有更高的ASCVD风险。肝功能正常的MAFLD患者可使用中等强度他汀类药物。血清丙氨酸氨基转移酶(ALT)或天门冬氨酸氨基转移酶(AST)升高在正常值上限3倍内且总胆红素水平正常者,可在原剂量或减量的基础上进行观察;如ALT或AST升高≥正常值上限3 倍,应停用他汀类药物;轻度肝功能受损(Child‑Pugh评分5~6分)患者可采用胆固醇吸收抑制剂或PCSK9抑制剂替代。失代偿性肝硬化和急性肝功能衰竭是他汀类药物的应用禁忌证,其他类型降脂药物在这些患者中的使用缺乏证据。
05
合并妊娠的患者
妊娠可导致血胆固醇水平生理性升高,LDL‑C水平可升高50%;患者妊娠期胆固醇水平异常升高将增加早产和胎儿动脉粥样硬化的风险。妊娠期的血脂管理重点是筛查以及饮食管理、合理运动、戒烟酒等生活方式改变,并将血糖控制在适宜范围,降脂药物的选择非常有限。
5 总结与展望
我国糖尿病患者人数居世界之首,有效管理糖尿病患者的血脂异常、降低心血管事件风险对于实施健康中国战略具有深远意义。对糖尿病患者进行ASCVD危险分层,针对不同危险分层确定血脂目标值和降脂治疗方案是糖尿病患者血脂管理的关键。在糖尿病患者血脂管理方面,尚有一些亟待解决的问题,包括降脂治疗靶标、新型降脂药物的随机对照研究、特殊人群的降脂治疗方案等。未来还需开展更多包括T1DM和T2DM患者在内的大规模、多中心临床研究,为糖尿病患者的血脂管理提供更多高质量的循证依据。